摘要:在慢性乙型和丙型肝炎病毒感染中,持续升高的抗原水平会驱使CD8+ T细胞走向一种被称为T细胞耗竭的特殊分化状态,这对抗病毒免疫产生了重要限制。现有证据表明,T细胞耗竭与一系列的代谢和信号调节失常以及一个非常特殊的表观遗传状态有关,这些共同导致效应器功能降低。关于细胞内代谢紊乱、转录和信号转导变化如何在T细胞耗竭分化特性的全面统一视图中相互连接的明确机制网络尚缺失。解决这个问题对于开发创新策略来增强宿主免疫以达到病毒清除的目的具有关键重要性。本文将讨论乙型和丙型肝炎病毒感染的当前知识,探讨如何针对固有免疫、代谢紊乱、广泛的应激反应和改变的表观遗传程序来恢复慢性病毒感染背景下特异性CD8 T细胞的功能和反应性。 关键词:慢性肝炎;T细胞耗竭;免疫调节;乙型肝炎病毒;丙型肝炎病毒。
- 引言 慢性乙型肝炎(CHB)的治疗依赖于直接作用的抗病毒药物,这些药物可以抑制病毒的产生,但不能从肝脏中根除HBV,需要终身治疗[1]。因此,迫切需要寻找新的治疗策略,以实现对CHB的最终治愈。相反,目前用于慢性丙型肝炎的直接作用的抗病毒药物(DAA)在85-99%的病例中可以引发持续的病毒学应答,尽管仍然存在大量治疗失败的患者[2]。出于这些原因,本文旨在探讨最新的病毒发病机制衍生出来的针对慢性乙型和丙型肝炎的免疫调节的新观念。
在慢性乙型和丙型肝炎中,特异性T淋巴细胞被描述为深度功能障碍,其低反应状态的严重性至少在某种程度上取决于病毒血症和抗原血症的水平[3](图1)。
这种功能障碍状态被称为“T细胞耗竭”,其特点是由于持续暴露于高抗原浓度导致的CD8 T细胞的重复触发而逐渐失去T细胞效应器功能[4]。首次在小鼠的慢性LCMV感染中观察到,随后在不同的动物和人类慢性病毒感染以及癌症中描述[4]。已确定了不同程度的功能性T细胞损伤,其中IL-2产生、细胞毒活性、细胞因子多功能性和增殖能力首先丧失,随后是TNF-α和IFN-γ分泌,直至在耗竭的最终阶段出现物理性T细胞删除[5]。除了持续的抗原刺激外,还显示出其他外部因子,如增加的调节T细胞活性、抑制性细胞因子和CD4 T细胞帮助的丧失,已被证明促进T细胞功能障碍[6-9]。
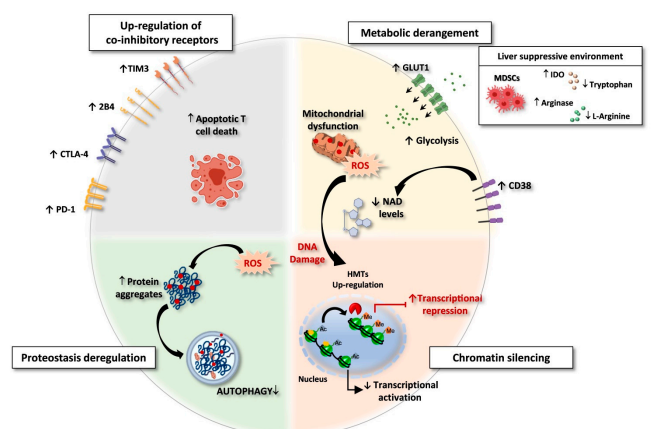
图1. HBV和HCV慢性感染中的耗竭CD8 T细胞。耗竭T细胞的特征如下:
(i) 多种共抑制受体的上调;
(ii) 代谢紊乱,伴随着去极化的线粒体和ROS的积累。富含氨基酸降解酶(例如,精氨酸酶和IDO/TDO)的抑制性肝内微环境导致氨基酸可用性减少。较低的呼吸能力和氨基酸饥饿有利于糖解作为一种代偿机制,伴随着葡萄糖转运蛋白GLUT-1的上调。此外,CD38的过度表达可能导致细胞内NAD消耗增加,加剧线粒体功能障碍。
(iii) 由于组蛋白甲基转移酶(HMTs)的上调以及由于低NAD水平导致的酰辅酶A(acetyl-CoA)可用性降低(NAD是组蛋白乙酰化的基本辅助因子)而导致染色质沉默。
(iv) 蛋白质稳态调控失常。高ROS水平导致蛋白质和细胞器的氧化和损伤。耗竭的CD8 T细胞表现出失调的蛋白质稳态,伴随着较低的自噬率,导致聚集的蛋白质和受损的细胞器的清除受损。
该图由BioRender.com创建,于2021年9月1日访问。
这种功能障碍状态被称为“T细胞耗竭”,其特点是由于持续暴露于高抗原浓度导致的CD8 T细胞的重复触发而逐渐失去T细胞效应器功能[4]。首次在小鼠的慢性LCMV感染中观察到,随后在不同的动物和人类慢性病毒感染以及癌症中描述[4]。已确定了不同程度的功能性T细胞损伤,其中IL-2产生、细胞毒活性、细胞因子多功能性和增殖能力首先丧失,随后是TNF-α和IFN-γ的分泌,直到在耗竭的最终阶段出现物理性T细胞删除[5]。除了持续的抗原刺激,还显示出其他外部因子,如增加的调节T细胞活性、抑制性细胞因子和CD4 T细胞帮助的丧失,已被证明促进T细胞功能障碍[6-9]。
从急性或慢性LCMV感染的小鼠中提取的病毒特异性CD8 T细胞的基因表达谱的比较,导致了在慢性感染中PD-1这一共抑制受体的高表达的发现,以及它在促进功能障碍表型中的作用[10]。后来,其他上调的抑制检查点的共同表达与耗竭的CD8 T细胞表型相关[6,11-13]。通常,被耗竭的T细胞共同表达的抑制性受体的数量越高,耗竭状态就越严重[11]。耗竭T细胞的其他特点是改变的转录程序、失调的代谢、记忆标志物的丧失、某些转录因子的上调,如Eomes和Blimp-1[14],与高Eomes表达相关的严重T细胞耗竭[15]。然而,最近已经证明,不仅是Eomes的表达,而且其亚细胞定位影响T细胞的耗竭程度:当Eomes存在于细胞核内时,它通过与转录因子Tbet竞争结合到Tbox序列来调节PD-1的表达。因此,高Eomes:Tbet比值可以增强PD-1的表达,因为Eomes是比Tbet弱的PD-1抑制剂。
从早期观察开始,发现在耗竭的LCMV特异性CD8 T细胞中,末端耗竭的PD-1hi和较少分化的PD-1int共存,逐渐明确耗竭的病毒特异性CD8 T细胞不能被认为是一个功能均一的功能障碍种群[17]。实际上,在慢性病毒感染的不同模型中,已经检测到具有不同功能程度和对免疫调节干预不同敏感性的T细胞亚群。此外,最近的单细胞(sc) RNA-seq数据支持组织相关异质性的观点,显示耗竭的病毒特异性CD8 T细胞的转录组学特性可以受到它们分化的特定微环境的影响[18]。一个表达TCF1转录因子的耗竭T细胞亚群已被确定为具有类似记忆的特性和比其TCF1阴性同类更高的抑制性检查点阻断敏感性,它是由更多的末端耗竭T细胞组成[19,20]。在慢性乙型肝炎中,也观察到了不同程度耗竭的病毒特异性CD8 T细胞亚群[21,22],其中末端耗竭细胞并不代表乙型肝炎患者中患有肝细胞癌的病毒特异性种群的大多数,无论是在外周(个人沟通)还是在肝内/肿瘤内水平[23]。此外,已经为识别不同的HBV抗原的HBV特异性CD8 T细胞确定了各种程度的T细胞功能障碍[24]。值得注意的是,PD-1和CD127的表达水平可以用来识别一个PD-1low/-CD127high CD8 T细胞亚群,这些细胞对功能恢复更为敏感,预测体外对免疫调节治疗的反应,从而允许识别那些更可能从免疫调节中受益的患者。据报道,CD127、PD-1和TCF1的共表达也能在慢性丙型肝炎中识别出一个具有残余增殖潜能的病毒特异性CD8 T细胞亚群[25]。这种类似记忆的T细胞亚群在慢性感染的自然或抗病毒治疗诱导的解决后得以维持,表明经过长时间的HCV暴露后的恢复不能导致规范记忆T细胞的表型和功能特性的完全重新获得[25]。与此观察一致,病毒特异性T细胞在慢性HBV和HCV感染解决后保持一个“分子疤痕”,而在急性肝炎的自然控制后不再持续[26-30]。 尽管在完全抗原清除后严重的耗竭可能不完全可逆,但功能恢复显然可以在较少的末端耗竭T细胞上实现,这表明免疫调节仍然可能是对抗慢性HBV和HCV感染的策略。
基于这些前提,本文将重点讨论已在体外或体内针对慢性乙型和丙型肝炎进行测试的提议的免疫调节方法(图2及表1和2),目标包括:
- 先天免疫受体
- 共抑制分子
- 代谢途径
- 细胞因子功能
- DNA转录的表观遗传控制
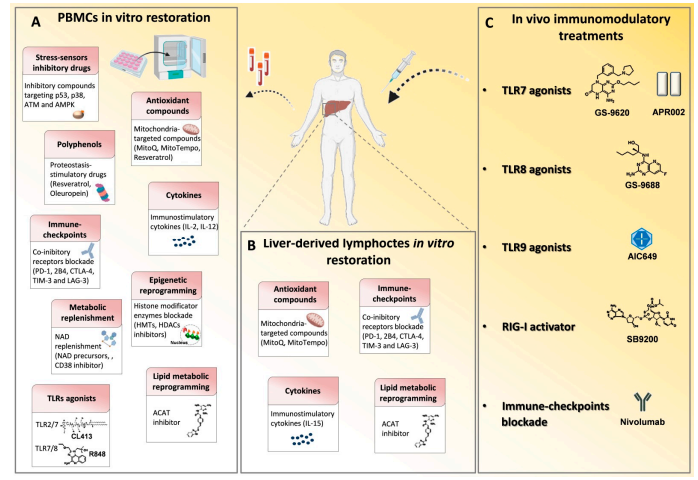
本图表描述了针对慢性HBV和HCV感染的基于免疫的治疗方法。
(A) 体外T细胞调节治疗: 使用来自患者的PBMCs (外周血单核细胞) 进行测试的治疗方法,目的是恢复信号解调、细胞因子水平、代谢功能和表观遗传景观,并阻断抑制性受体信号。
(B) 体外肝源性淋巴细胞的治疗: 类似于(A)部分,但是来源于肝脏的淋巴细胞。
(C) 体内T细胞功能重建: 这些治疗目标是激活天然免疫受体,例如Toll样受体 (TLRs) 和retinoic acid-inducible gene 1 (RIG-I),通过特定的激动剂和通过检查点阻断,例如使用抗PD-1单克隆抗体(Nivolumab)。
此外,还列举了多种与免疫调节相关的重要分子和蛋白,包括:
- p53: 肿瘤抑制蛋白
- p38: 丝裂原活化的蛋白激酶
- ATM: 先天性毛细血管扩张突变
- AMPK: AMP活化的蛋白激酶
- MitoQ: 一种线粒体靶向的抗氧化剂
- MitoTempo: 一种线粒体靶向的超氧化物歧化酶
- PD-1: 细胞程序性死亡蛋白1
- 2B4: 天然杀伤细胞受体2B4
- CTLA4, TIM3, LAG3: 抑制性免疫受体
- HMTs: 组蛋白甲基转移酶
- HDACs: 组蛋白去乙酰化酶
- NAD 和 NMN: 与细胞代谢和红ox平衡相关的小分子
- ACAT: 醋酰辅酶A醋酰转移酶,参与脂质代谢。
- 刺激先天免疫受体作为克服HBV特异性T细胞耗竭的免疫调节策略
在为慢性HBV感染开发新疗法的可能策略中,通过刺激如Toll样受体(TLRs)、视黄醇酸诱导基因1(RIG-I)和干扰素基因刺激因子(STING)之类的先天免疫受体来重建抗病毒T细胞功能,代表了在CHB患者中恢复保护性免疫的潜在途径[71](图2及表1和2)。这些制剂旨在刺激模式识别受体,最终导致具有抗病毒活性的细胞因子(例如,干扰素)的产生,其最终目的是以非抗原特异性方式激活宿主免疫。TLRs位于细胞表面或内质网内,它们感知与病毒和细菌相关的分子模式。
最近描述了许多通过TLR7激活来刺激先天免疫的尝试[31]。TLR7主要在B淋巴细胞和浆细胞样树突状细胞的内质网膜上表达,其刺激导致转录因子NFkB和IRF7的激活。
最近的研究表明,TLR7激动剂GS-9620在黑猩猩和土拨鼠中显示出持续的抗病毒反应[32,33]。Boni等人对人类进行的进一步研究表明,TLR7刺激可以增强NK和T细胞在由核苷(酸)类似物(NUC)诱导的HBV复制抑制的慢性患者中的反应[34]。尽管TLR7刺激提高了NUC对T细胞反应的效果,但这不足以允许获得足够的免疫反应,以提供完全的感染控制,如在自然控制的自限性急性感染后可检测到。这种在CHB患者中的治疗效果不佳可以广泛地解释为为避免可能的毒性效应,在人类中使用的药物剂量非常低。最近,一种新的TLR-7激活剂,名为APR002,已经单独使用或与Entecavir(ETV)结合在土拨鼠感染模型中使用。重要的是,由于有机转运多肽1B1/3转运体在肝细胞上高度表达,这种化合物显示出优先的肝内给药。由于这种肝选择性,APR002在土拨鼠肝脏中高度定位,最大限度地减少了全身暴露,并促进了慢性肝炎动物的持续病毒控制[35,36]。
- 刺激先天免疫受体作为克服HBV特异性T细胞耗竭的免疫调节策略
TLR8是模式识别受体家族的另一个成员,主要在髓样树突状细胞(DCs)、单核细胞、巨噬细胞和T调节细胞中表达。最近,很多关注都集中在内质网TLR8的激动剂GS-9688(Selgantolimod)上,其刺激导致免疫调节(例如,IL-12、IL-18)和促炎细胞因子(例如,IL-1β、TNF-α)的产生,最终引发肝脏驻留细胞的强烈IFN-γ产生。通过这些效应,激动剂诱导的TLR-8激活在HBV感染的初级人肝细胞中体外以及在土拨鼠中慢性感染的土拨鼠肝炎病毒(WHV)中体内均显示出抗病毒效应[37,38]。通过研究其对健康受试者和CHB患者的人体免疫细胞的体外效应,提供了对GS-9688作用机制的进一步见解。TLR8刺激激活DCs和单核吞噬细胞产生IL-12和TNF-α,增加了CHB患者中功能性HBV特异性CD8 T细胞的频率,激活了NK细胞、黏膜相关的不变T细胞(MAITs),并减少了T调节细胞和髓源性抑制细胞(MDSC)的频率[39]。在1b期研究中评估了Selgantolimod的安全性、药代动力学和药效动力学,在CHB患者中,显示了良好的耐受性和血清IL-12和IL-1RA的瞬时剂量依赖性增加,这暗示了可能对免疫反应的影响[40]。 有趣的是,双作用TLR7/8(R848)和TLR2/7(CL413)激动剂被描述为有效的抗病毒细胞因子的广谱诱导剂,能够有效地抑制HBV感染的初级人肝细胞中的HBV产生,从而为多特异性TLR激动剂治疗提供了合理性,作为HBV治疗的新方法[41]。 更近期,新的免疫调节剂AIC649,一种能够通过TLR9途径刺激先天免疫的灭活的细胞瘤病毒基粒,与Entecavir结合后在土拨鼠慢性肝炎模型中显著降低了病毒DNA和WHsAg。肝脏中的病毒复制的抑制与I型和II型干扰素的肝内表达相关[42]。最近的报告强调了TLR9信号作为一种新的刺激途径的重要性,这种报告证明了用CpG寡核苷酸进行的宿主调节可以恢复耗竭的肝脏CXCR5+ CD8 T细胞,
- 通过阻断共抑制途径增强适应性免疫反应
许多体外研究已广泛描述了HBV特异性CD8 T细胞耗竭中共抑制分子的作用,这些研究涉及外周和肝内病毒特异性CD8 T细胞(图2,表1和表2)。实际上,在慢性HBV感染中,流通的病毒特异性CD8 T细胞的特点是上调了几种抑制性受体,如PD-1、2B4、CTLA-4、TIM-3和LAG-3,PD-1在肝浸润的HBV特异性T淋巴细胞中的最大表达[45,46,53–56](图1)。
如先前在其他慢性病毒感染中(如LCMV和HCV)报告的那样[4,19,20,25,26,74,75],也有耗竭的HBV特异性CD8 T细胞是由具有不同耗竭程度的不同亚群组成的异质种群,根据不同的HBV抗原特异性共同存在[21,22,24,27,76]。由于这种异质性,其他T细胞耗竭模型中报告的病毒特异性CD8 T细胞显示出对免疫恢复治疗的可变敏感性[19,20,77–80]。因此,基于其功能障碍程度识别那些更有可能受益于免疫治疗的患者可能是选择最佳候选人进行功能T细胞恢复治疗的有用策略。
PD-1是在肿瘤和慢性病毒感染中研究最广泛的抑制性受体,目前,在慢性HBV感染领域,旨在阻断PD-1/PD-L1途径的策略是体外、动物模型和慢性感染患者中研究最多的治疗选择。阻断PD-1/PD-L1轴的药物已被描述为增强HBV特异性T细胞反应,在许多体外研究中,显示了在肝内比在外周部位更高的改善水平[46,47,53]。然而,由PD-1/PD-L1封锁诱导的T细胞功能恢复,即使与调节其他共抑制或共刺激途径(如CTLA-4、CD137、TIM-3、2B4)的组合,也只在有限比例的CHB患者中观察到,T细胞反应性的广泛异质性[45,54–56]。有趣的是,观察到OX40刺激与PD-L1封锁结合后,IFN-γ和IL-21产生的HBV特异性CD4 T细胞的分泌增加,这表明免疫治疗方法还可以改善HBV特异性CD4 T细胞反应[57]。
ETV治疗、DNA疫苗和体内PD-L1封锁的三重组合疗法已在WHV感染的土拨鼠中报道,以增强病毒特异性T细胞反应,导致WHsAg的丧失和病毒复制的减少[48,49]。在一项更近期的研究中,WHV感染的土….